
Une bonne nouvelle dans l’avancée vers un médicament pour la myopathie FSHD !
Ce qu’il faut comprendre de l’essai
Un nouvel essai clinique de phase I/II vient d’être lancé par le laboratoire Epicrispr Biotechnologies. Son médicament (EPI-321 du type CrispR véhiculé par un virus désactivé) doit rétablir la méthylation de la fin du chromosome 4 pour empêcher l’expression de DUX4.
- EPI-321 est une thérapie d’édition épigénétique visant à inhiber l’expression de DUX4 sans couper l’ADN, et ainsi s’attaquer à la cause génétique de la dystrophie Facio-Scapulo-Humérale. Elle est administrée en une seule perfusion intraveineuse via un vecteur AAVrh74*, capsule virale inoffensive et désactivée utilisée comme véhicule pour livrer le traitement jusqu’aux cellules musculaires
- L’essai de phase 1/2 (première partie en phase 1) a démarré : premier patient traité le 5 août 2025. Des premiers résultats sont attendus début 2026
- L’étude est ouverte sur 9 participants avec un suivi jusqu’à 5 ans dans trois pays : États-Unis (Géorgie), Australie (Sydney) et Nouvelle-Zélande (Auckland)
- EPI-321 bénéficie des statuts FDA Orphan Drug, Fast Track et Rare Pediatric Disease qui peuvent accélérer son développement
Pourquoi s’attaquer à DUX4 ?
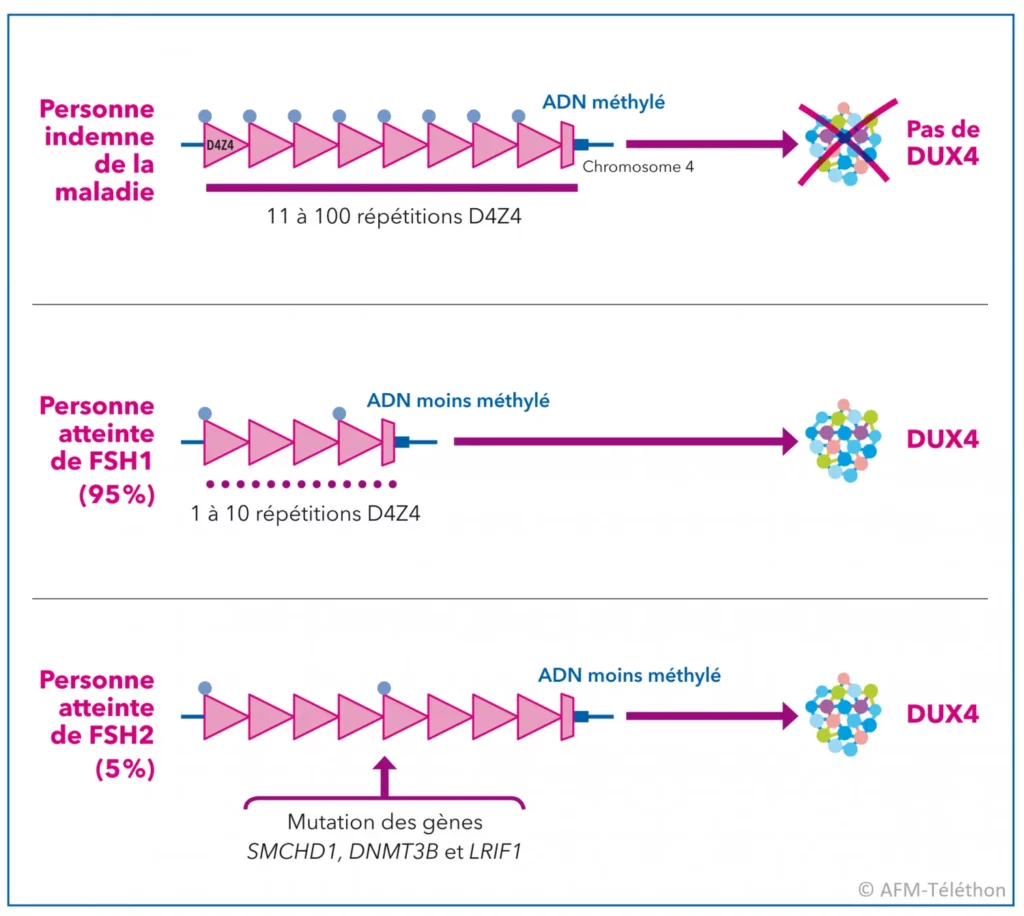
Comme vous le savez peut-être déjà, la cause la plus probable de la myopathie FSHD est la relaxation de la chromatine par hypométhylation dans le chromosome 4. Résultat : le gène DUX4 peut s’exprimer et produit une protéine toxique responsable des lésions musculaires. L’EPI-321 agit au niveau épigénétique. L’objectif est de réinstaller des “verrous épigénétiques”; autrement dit remettre de la méthylation au bon endroit pour empêcher DUX4 de s’exprimer.
Comment fonctionne EPI-321 ?
Pensez à l’ADN comme à une bibliothèque : les gènes sont des livres. Dans un muscle sain, le livre “DUX4” est rangé sous clé. Dans la FSHD, la clé est perdue : le livre s’ouvre et se met à “parler”.
EPI-321 utilise un outil CRISPR “non coupant” (dCas) couplé à des modulateurs épigénétiques : il ne réécrit pas le livre, il remet la serrure.
Objectif : fermer durablement DUX4 pour empêcher la production de protéines toxiques.
En quoi consiste l’essai ?
- Autorisation : le laboratoire a obtenu une autorisation rapide de la FDA (Food and Drug Administration) aux USA et le statut de médicament orphelin.
- Traitement : une seule injection.
- Nombre de patients : 9 adultes FSHD1
- Type d’étude : escalade de dose (2 niveaux) avec pour objectif la sécurité et la tolérance du traitement sur les 1ers patients + observation des signaux biologiques
- Suivi : visites régulières jusqu’à 5 ans après la perfusion
- Où : aux USA, en Australie et en Nouvelle-Zélande
- Ce que mesure les équipes par biopsies musculaires : DUX4 et ses marqueurs, la méthylation de la région D4Z4 et l’activité ‘cargo’ EPI-321 et les copies de vecteur dans le muscle
Calendrier
- Premier patient traité : 05 août 2025
- Premiers résultats : début 2026
En savoir plus
*Que signifie Vecteur AAVrh74 ?
- AAV = adeno-associated virus (virus adéno-associé). Dans les thérapies géniques, on utilise une version recombinée et inoffensive de ce virus comme véhicule pour livrer le traitement jusqu’aux cellules.
- rh74 désigne une variante d’AAV qui cible particulièrement bien le muscle
- Le “vecteur” est une coquille virale vidée de ses propres gènes et incapable de se multiplier. On y met à la place les instructions thérapeutiques. Il sert de navette : il entre dans les cellules musculaires et y dépose sa cargaison.
À propos d’Epicrispr Biotechnologies
Epicrispr Biotechnologies est une société de biotechnologie pionnière dans les thérapies modulatrices géniques, leader dans le traitement des maladies neuromusculaires. Son système exclusif de modulation de l’expression génique (GEMS) permet un contrôle précis et durable de l’expression génique, ouvrant la voie à des traitements innovants pour des maladies jusqu’alors incurables. Le programme phare Epicrispr EPI-321 est en phase d’essais cliniques pour la FSHD, et l’entreprise développe d’autres thérapies modulatrices géniques.
Réponses aux questions fréquentes
- L’ADN est-il modifié ?
Non. L’outil CRISPR utilisé est “non coupant” : il règle l’expression du gène (épigénétique) sans changer la séquence.
- Une perfusion suffit-elle à vie ?
Nous ne savons pas encore. L’objectif est une suppression durable de l’expression de DUX4. Seul le suivi à long terme dira si l’effet persiste et si une seconde dose est souhaitable/possible.
- Y a-t-il des risques spécifiques à cet essai ?
Comme toute thérapie génique AAV, les réactions immunitaires, l’atteinte hépatique, les effets liés au vecteur sont hautement surveillés. C’est précisément l’objet d’une phase 1 : évaluer la sécurité et la tolérance sur l’être humain.
- Puis-je participer depuis la France à cet essai ?
L’essai se déroule actuellement aux États-Unis, en Australie et en Nouvelle-Zélande. Des critères stricts s’appliquent (dont les anticorps anti-AAVrh74). Aucun centre en France à ce jour n’est répertorié.
Votre Groupe d’Intérêt FSHD reste à votre écoute pour répondre à vos questions :
fshd@afm-telethon.fr








Bonjour je suis ravie d apprendre cette bonne nouvelle. C est un grand début et une grande avancée pour la recherche du traitement. Hâte d avoir des nouvelles plus pour mes petites nièces que pour moi .
Merci de nous tenir régulièrement au courant ça fait du bien.
Bonjour,cela est d’un grand réconfort de voir que la science avance étant atteinte de la fsh type 1 ,ainsi que mon fils . Espérant que ce sera concluant.Merci de m’informer de l’évolution des recherches bon courage à tous.